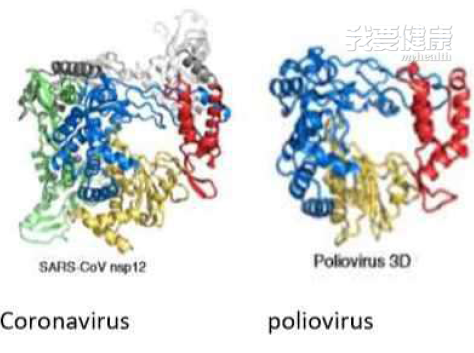
HWGB Biotech 对寻求疫苗的贡献
RECENT POSTS
摆脱膝关节炎折磨 自己的膝盖自己救
2023年12月29日
鼻窦炎·鼻炎 满腔鼻涕寻纸巾
2023年11月28日
骨痛热症 5个常见误解
2023年11月27日
马中企业家大健康产业论坛 汇集各领域专家促进双边合作
2023年11月27日
复健机器人 助力患者破茧重生
2023年11月24日
立丰媒体有限公司
REVON MEDIA SDN. BHD.
201701042052 (1256225-D)
A-5-1, Parklane Commercial Hub,
Jalan SS 7/26, SS 7,
47301 Petaling Jaya,
Selangor D.E., Malaysia.
Tel: +603-7886 6091
Email : myhealth@revonmedia.com
A member of Revongen Corporation

深受认可 AWARD WINNING
2018年金医奖“最杰出健康与时尚媒体奖”
The Best Health and Lifestyle Media Award
2019年金医奖“最杰出健康与时尚媒体奖”
The Best Health and Lifestyle Media Award
Menu
立丰媒体有限公司
REVON MEDIA SDN. BHD.
201701042052 (1256225-D)
Level 17, Top Glove Tower,
No. 16, Persiaran Setia Dagang,
Bandar Setia Alam, Seksyen U13, 40170 Shah Alam, Selangor D.E., Malaysia.
Tel: +603 – 3359 1166
Fax: +603 – 3358 0303
Email : myhealth@revonmedia.com
A member of Revongen Corporation


深受认可 AWARD WINNING
2018年金医奖“最杰出健康与时尚媒体奖”
The Best Health and Lifestyle Media Award
2019年金医奖“最杰出健康与时尚媒体奖”
The Best Health and Lifestyle Media Award
Menu